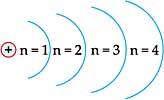Modelos Atômicos: Dalton, Thomson, Rutherford
A constituição da matéria sempre foi motivo de grande curiosidade entre os povos, sejam eles antigos, ou os atuais. Filósofos buscaram por muito tempo entender a constituição dos materiais. Consequentemente, acabaram por descobrir o fogo, o que permitiu cozinhar os alimentos, além de contribuir no desenvolvimento da sociedade.
A partir dessa descoberta pôde-se verificar, ainda, que o minério de cobre (conhecido na época com pedras azuis), quando submetido ao aquecimento, produzia cobre metálico, ou aquecido na presença de estanho, formava o bronze.
Dessa forma, conclui-se que a passagem do homem pelas “idades” da pedra, do bronze e do ferro, foi de muito aprendizado para o homem, pois lhe permitiu produzir materiais úteis.
Os primeiros conceitos teóricos da Química surgiram a partir de 400 a.C.. Filósofos gregos, como Demócrito e Leucipo, chegaram a afirmar que a matéria não era contínua, e sim constituída por minúsculas partículas indivisíveis, às quais deram o nome de átomos. Platão e Aristóteles, que eram filósofos muito influentes na época, recusaram tal proposta e defendiam a ideia de matéria contínua.
Esse conceito de Aristóteles permaneceu até a Renascença, quando por volta de 1650 d.C. o conceito de átomo foi novamente proposto por Pierre Cassendi, filósofo francês.
O conceito de “Teoria atômica” veio a surgir após a primeira ideia científica de átomo, proposta por John Dalton após observações experimentais sobre gases e reações químicas.
Os modelos atômicos são, portanto, teorias fundamentadas na experimentação. Tratam-se, portanto, de explicações para mostrar o porquê de um determinado fenômeno. Diversos cientistas desenvolveram suas teorias até que se chegou ao modelo atual.
1. Modelo Atômico de Dalton
Em 1808, o professor inglês John Dalton propôs uma explicação da natureza da matéria. A proposta foi baseada em fatos experimentais. Os principais postulados da teoria de Dalton são:
1. “Toda matéria é composta por minúsculas partículas chamadas átomos”.
2. “Os átomos de um determinado elemento são idênticos em massa e apresentam as mesmas propriedades químicas”.
3. “Átomos de diferentes elementos apresentam massa e propriedades diferentes”.
4. “Átomos são permanentes e indivisíveis, não podendo ser criados e nem destruídos”.
5. “As reações químicas correspondem a uma reorganização de átomos”.
6. “Os compostos são formados pela combinação de átomos de elementos diferentes em proporções fixas”.
A conservação da massa durante uma reação química (Lei de Lavoisier) e a lei da composição definida (Lei de Proust) passou a ser explicada a partir desse momento, por meio das ideias lançadas por Dalton.
2. Modelo Atômico de Thomson
Pesquisando sobre raios catódicos e baseando-se em alguns experimentos, J.J. Thomson propôs um novo modelo atômico. Thomson demonstrou que esses raios podiam ser interpretados como sendo um feixe de partículas carregadas de energia elétrica negativa. A essas partículas denominou-se elétrons. Por meio de campos magnético e elétrico pôde-se determinar a relação carga/massa do elétron.
Consequentemente, concluiu-se que os elétrons (raios catódicos) deveriam ser constituintes de todo tipo de matéria pois observou que a relação carga/massa do elétron era a mesma para qualquer gás empregado. O gás era usado no interior de tubos de vidro rarefeitos denominadas Ampola de Crookes, nos quais se realizavam descargas elétricas sob diferentes campos elétricos e magnéticos.
Esse foi o primeiro modelo a divisibilidade do átomo, ficando o modelo conhecido como “pudim de passas”. Segundo Thomson, o átomo seria um aglomerado composto de uma parte de partículas positivas pesadas (prótons) e de partículas negativas (elétrons), mais leves.
3. Modelo Atômico de Rutherford
Em 1911, Ernest Rutherford, estudando a trajetória de partículas a (partículas positivas) emitidas pelo elemento radioativo polônio, bombardeou uma fina lâmina de ouro.
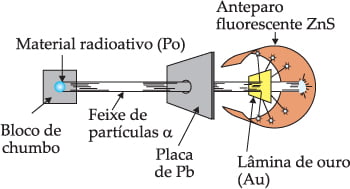
Ele observou que:
– a maioria das partículas a atravessavam a lâmina de ouro sem sofrer desvio em sua trajetória. Logo, há uma grande região de vazio, que passou a se chamar eletrosfera;
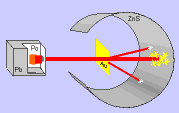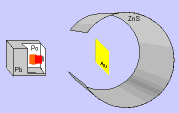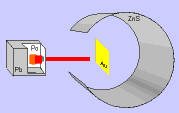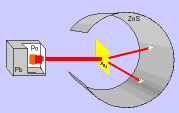
– algumas partículas sofriam desvio em sua trajetória: haveria uma repulsão das cargas positivas (partículas a) com uma região pequena também positiva (núcleo).
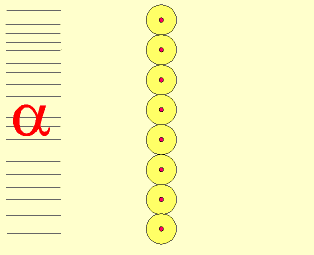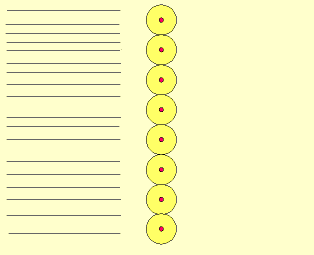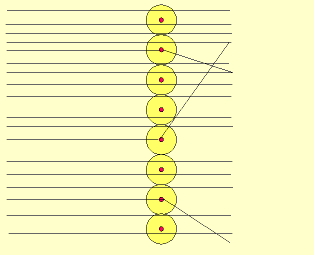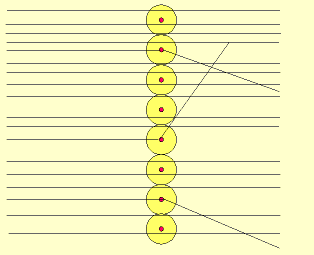
– um número muito pequeno de partículas batiam na lâmina e voltavam (portanto, a região central é pequena e densa, sendo composta portanto, por prótons).
Diante das observações, Rutherford concluiu que a lâmina de ouro seria constituída por átomos formados com um núcleo muito pequeno carregado positivamente (no centro do átomo) e muito denso, rodeado por uma região comparativamente grande onde estariam os elétrons.
Nesse contexto, surge ainda a ideia de que os elétrons estariam em movimentos circulares ao redor do núcleo, uma vez que se estivesse parados, acabariam por se chocar com o núcleo, positivo.
O pesquisador acreditava que o átomo seria de 10000 a 100000 vezes maior que seu núcleo.
4. Modelo Atômico Clássico
As partículas presentes no núcleo, chamadas prótons, apresentam carga positiva. A partícula conhecida como nêutron foi isolada em 1932 por Chadwick, embora sua existência já fosse prevista por Rutherford.
Dessa forma, o modelo atômico clássico constitui-se de um núcleo, no qual se encontram os prótons e nêutrons, e de uma eletrosfera, na qual estão os elétrons girando ao redor do núcleo em órbitas.
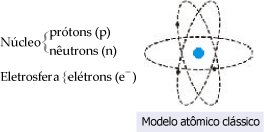
Considerando-se a massa do próton como padrão, observou-se que sua massa era aproximadamente igual à massa do nêutron e 1836 vezes maior que o elétron. Logo:
![]()
A essas três partículas básicas, prótons, nêutrons e elétrons, é comum denominar partículas elementares ou fundamentais.
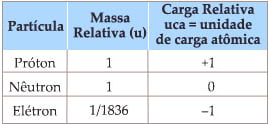
Algumas características físicas das partículas atômicas fundamentais:
Modelo Atômico Rutherford-Bohr
O modelo proposto por Rutherford foi aperfeiçoado por Bohr. Baseando-se nos estudos feitos em relação ao espectro do átomo de hidrogênio e na teoria proposta por Planck em 1900 (Teoria Quântica), segundo a qual a energia não é emitida em forma contínua, mas em ”pacotes”, denominados quanta de energia. Foram propostos os seguintes postulados:
1. Na eletrosfera, os elétrons descrevem sempre órbitas circulares ao redor do núcleo, chamadas de camadas ou níveis de energia.
2. Cada camada ocupada por um elétron possui um valor determinado de energia (estado estacionário).
3. Os elétrons só podem ocupar os níveis que tenham uma determinada quantidade de energia, não sendo possível ocupar estados intermediários.
4. Ao saltar de um nível para outro mais externo, os elétrons absorvem uma quantidade definida de energia (quantum de energia).
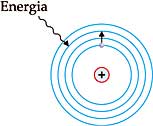
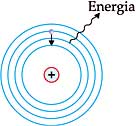
5. Ao retornar ao nível mais interno, o elétron emite um quantum de energia (igual ao absorvido em intensidade), na forma de luz de cor definida ou outra radiação eletromagnética (fóton).
6. Cada órbita é denominada de estado estacionário e pode ser designada por letras K, L, M, N, O, P, Q. As camadas podem apresentar:
K = 2 elétrons
L = 8 elétrons
M = 18 elétrons
N = 32 elétrons
O = 32 elétrons
P = 18 elétrons
Q = 2 elétrons
7. Cada nível de energia é caracterizado por um número quântico (n), que pode assumir valores inteiros: 1, 2, 3, etc.
NOTA DE CORTE SISU
Clique e se cadastre para receber as notas de corte do SISU de edições anteriores.