Questões sobre Estequiometria: Volume de Gases
01) (UFRGS/2018) A decomposição térmica do ácido nítrico na presença de luz libera NO2 de acordo com a seguinte reação (não balanceada).
HNO3(aq) → H2O(l) + NO2(g) + O2(g)
Assinale a alternativa que apresenta o volume de gás liberado, nas CNTP, quando 6,3 g de HNO3 são decompostos termicamente.
a) 2,24 L
b) 2,80 L
c) 4,48 L
d) 6,30 L
e) 22,4 L
02) (UPF/2018) Tendo por referência a reação química não balanceada
Cl2(g) + O2(g) → Cl2O5(s)
qual é o volume de oxigênio necessário para reagir com todo o cloro, considerando-se que se parte de 20 L de cloro gasoso medidos em condições ambientes de temperatura e pressão?
(Considere volume molar de 25 mol.L-1 nas CNTP)
a) 20 L.
b) 25 L.
c) 50 L.
d) 75 L.
e) 100 L
03) (UERJ/2018) A hemoglobina é uma proteína de elevada massa molar, responsável pelo transporte de oxigênio na corrente sanguínea. Esse transporte pode ser representado pela equação química abaixo, em que HB corresponde à hemoglobina.
HB + 4O2 → HB(O2)4
Em um experimento, constatou-se que 1 g de hemoglobina é capaz de transportar 2,24 x 10-4 L de oxigênio molecular com comportamento ideal, nas CNTP. A massa molar, em g/mol, da hemoglobina utilizada no experimento é igual a:
a) 1 x 105
b) 2 x 105
c) 3 x 105
d) 4 x 105
Gabarito das Questões sobre Estequiometria envolvendo Volume de Gases
01) Resp.: B

02) Resp.: C

03) Resp.: C
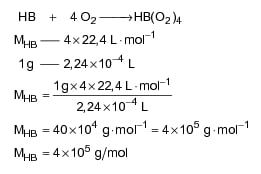
NOTA DE CORTE SISU
Clique e se cadastre para receber as notas de corte do SISU de edições anteriores.
Agora sua informação está no WhatsApp!
Siga nosso canal e receba as notícias mais importantes do dia! CONHECER ➔



