Questões do Enem sobre Pilhas
01) ENEM Digital (2020) As populares pilhas zinco-carbono (alcalinas e de Leclanché) são compostas por um invólucro externo de aço (liga de ferro-carbono), um ânodo (zinco metálico), um cátodo (grafita) e um eletrólito (MnO2 mais NH4Cl ou KOH), contido em uma massa úmida com carbono chamada pasta eletrolítica. Os processos de reciclagem, geralmente propostos para essas pilhas usadas, têm como ponto de partida a moagem (trituração). Na sequência, uma das etapas é a separação do aço, presente no invólucro externo, dos demais componentes.
Que processo aplicado à pilha moída permite obter essa separação?
a) Catação manual
b) Ação de um eletroímã
c) Calcinação em um forno
d) Fracionamento por densidade
e) Dissolução do eletrólito em água
02) Enem digital (2020) As pilhas recarregáveis, bastante utilizadas atualmente, são formadas por sistemas que atuam como uma célula galvânica, enquanto estão sendo descarregadas, e como célula eletrolítica, quando estão sendo recarregadas.
Uma pilha é formada pelos elementos níquel e cádmio e seu carregador deve fornecer uma diferença de potencial mínima para promover a recarga. Quanto maior a diferença de potencial gerada pelo carregador, maior será o seu custo. Considere os valores de potencial padrão de redução dessas espécies:
Ni2+(aq) + 2 e− ⇌ Ni (s) E° = −0,230 V
Cd2+(aq) + 2 e− ⇌ Cd (s) E° = −0,402 V
Teoricamente, para que um carregador seja ao mesmo tempo eficiente e tenha o menor preço, a diferença de potencial mínima, em volt, que ele deve superar é de
a) 0,086.
b) 0,172.
c) 0,316.
d) 0,632.
e) 1,264.
03) ENEM cancelado 2018 Em 1938 o arqueólogo alemão Wilhelm König, diretor do Museu Nacional do Iraque, encontrou um objeto estranho na coleção da instituição, que poderia ter sido usado como uma pilha, similar às utilizadas em nossos dias. A suposta pilha, datada de cerca de 200 a.C., é constituída de um pequeno vaso de barro (argila) no qual foram instalados um tubo de cobre, uma barra de ferro (aparentemente corroída por ácido) e uma tampa de betume (asfalto), conforme ilustrado. Considere os potenciais-padrão de redução: E θ(Fe2+|Fe) = –0,44 V; E θ(H+|H2) = 0,00 V; e E θ(Cu2+|Cu) = +0,34 V.
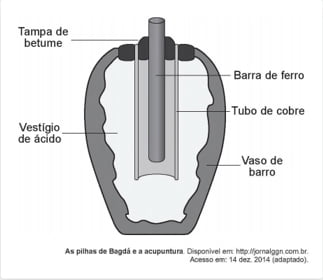
Nessa suposta pilha, qual dos componentes atuaria como cátodo?
a) A tampa de betume.
b) O vestígio de ácido.
c) A barra de ferro.
d) O tubo de cobre.
e) O vaso de barro.
Resolução das Questões do Enem sobre Pilhas
01) A ação de um eletroímã ou separação magnética permite a retirada das partículas ferromagnéticas da mistura heterogênea sólida.
Resp.: B
02) Observando os valores de potencial de redução fornecidos, verifica-se que o íon Ni2+(aq) apresenta um maior potencial padrão de redução, assim o eletrodo de níquel será o cátodo e o eletrodo de cádmio será o ânodo.
Dessa forma, o potencial padrão da pilha será:
∆E° = E°cátodo – E°ânodo
∆E° = -0,230 – (- 0,402)
∆E° = 0,172 V
Resp.: B
03) Uma pilha é formada por ânodo e cátodo. O ânodo é o polo negativo da pilha, onde ocorre a oxidação e os elétrons migram a partir dele. O cátodo é o polo positivo da pilha, onde ocorre a redução e os elétrons serão recebidos.
Os potenciais-padrão de redução dados na questão nos dizem qual substância tem a maior facilidade em reduzir (ganhar elétrons) entre os metais.
E θ(Fe2+|Fe) = –0,44 V
E θ(H+|H2) = 0,00 V
E θ(Cu2+|Cu) = +0,34 V
Quem possui o maior potencial de redução é o cobre, ou seja, espontaneamente tem a tendência de receber elétrons. Logo, o tubo de cobre atua como cátodo.
Resp.: D
NOTA DE CORTE SISU
Clique e se cadastre para receber as notas de corte do SISU de edições anteriores.
Agora sua informação está no WhatsApp!
Siga nosso canal e receba as notícias mais importantes do dia! CONHECER ➔


